- Home
- Messverfahren
- Gamma-Spektrometrie
- Einsteiger
- Was ist Gamma-Spektrometrie?
Was ist Gamma-Spektrometrie?
Beginnen wir mit dem Begriff Gamma-Spektrometrie. Oftmals wird dafür auch der Begriff Gamma-Spektroskopie verwendet, was aber nicht wirklich korrekt ist, wie wir später noch erklären werden.
Der Begriff Gamma-Spektrometrie setzt sich aus den beiden Begriffen Gamma und Spektrometrie zusammen. Dabei steht Gamma abgekürzt für Gamma-Strahlung. Was man unter den beiden Begriffen versteht, wollen wir uns jetzt im Einzelnen näher ansehen. Lassen sie uns mit der Gamma-Strahlung beginnen.
Gamma-Strahlung
Wie Sie vielleicht schon wissen, besteht jeder materielle Stoff aus einzelnen Atomen. Falls Sie beispielsweise gerade eine Tasse Kaffee vor sich stehen haben während Sie durch diese Seiten blättern, dann besteht diese Tasse vermutlich hauptsächlich aus Silizium- und Sauerstoffatomen, ihr Kaffee aus Wasserstoff-, Sauerstoff-, Kohlenstoff-, Stickstoff- und weiteren Atomen. Auch Sie selbst bestehen aus Atomen: unter anderem zu etwa 96 % aus den Atomen Sauerstoff, Kohlenstoff, Wasserstoff und Stickstoff.
Jedes einzelne Atom setzt sich aus verschiedenen Teilchen zusammen, den Protonen, Neutronen und Elektronen. Die Protonen und Neutronen bilden den Atomkern, die Elektronen befinden sich in der Atomhülle, welche den Kern umgibt. Die Anzahl an Protonen, die ein einzelnes Atom besitzt, wird als Ordnungszahl oder Kernladungszahl bezeichnet. Sie definiert unter anderem die chemischen Eigenschaften eines Atoms.
Vielleicht ist Ihnen in diesem Zusammenhang auch schon der Begriff eines Elements untergekommen. Dabei handelt es sich um eine reine Substanz, die vollständig aus einer Art von Atomen besteht. So besteht beispielsweise das Element Kohlenstoff aus Atomen, die alle die Kernladungszahl 6, d. h. 6 Protonen haben. Die folgende Liste zeigt einige Beispiele für Kernladungszahlen und den zugehörigen Elementbezeichnungen.
Liste mit Beispielen für Kernladungszahlen und den zugehörigen Elementbezeichnungen.
| Anzahl an Protonen (Kernladungszahl) | Elementbezeichnung |
|---|---|
|
1 |
Wasserstoff |
|
6 |
Kohlenstoff |
|
7 |
Stickstoff |
|
8 |
Sauerstoff |
|
14 |
Silizium |
Eine Liste aller Elementnamen mit der Kernladung 1 bis 84 findet sich hier.
Anmerkung:
Die Kerne von spezifischen Elementen (z.B. Wasserstoff, Kohlenstoff, …) werden als Nuklide bezeichnet.
Warum haben wir uns jetzt so lange mit Atomen, Protonen, Neutronen, Kernladungszahl etc. befasst, wenn wir doch wissen wollen, was es mit dem Begriff Gamma-Strahlung auf sich hat?
Nun, hier kommt der sogenannte radioaktive Zerfall ins Spiel. Und wir müssen uns auch noch die Neutronen ansehen, die in einem Atomkern neben den Protonen enthalten sind.
Beginnen wir mit den Neutronen: Wir wissen bereits, dass sich ein Atomkern aus Protonen und Neutronen zusammensetzt. Die Anzahl der Protonen bestimmt die Element- bzw. Nuklidbezeichnung. Nun kann aber jedes Element unterschiedlich viele Neutronen besitzen. Das Element Kohlenstoff kann beispielsweise (u. a.) 6, 7 oder 8 Neutronen besitzen. Diese unterschiedlichen Kombinationen werden als Isotope des Elements Kohlenstoff bezeichnet. Addiert man die Anzahl an Protonen und Neutronen eines Elements dann wird der resultierende Wert als Massenzahl A bezeichnet.
Zwei Beispiele:
- Das oben genannte Element Kohlenstoff (C) (Kernladungszahl 6) kann 6, 7 oder 8 Neutronen besitzen. Die Massenzahlen der Isotope des Elements Kohlenstoff sind dann 12, 13 oder 14.
- Das Element Beryllium (Be) (Kernladungszahl 4) kann beispielsweise 3, 5 oder 8 Neutronen besitzen. Die Massenzahlen der Isotope des Elements Beryllium sind dann 7, 9 oder 12.
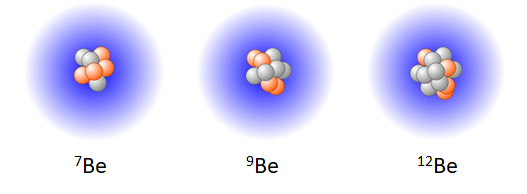
Schematische Darstellung von drei Beryllium-Isotopen mit den Massenzahlen 7, 9 und 12. Die Protonen sind rot, die Neutronen grau dargestellt.
Damit kommen wir zum radioaktiven Zerfall: Es gibt stabile Isotope und instabile Isotope. Die stabilen Isotope sorgen dafür, dass Sie Ihren Kaffee trinken können, ohne befürchten zu müssen, dass Ihre Kaffeetasse währenddessen plötzlich zerfällt (außer Sie lassen die Tasse selber fallen). Im Gegensatz hierzu zerfallen die instabilen Isotope nach einer gewissen Zeit. Hierbei ändert sich die Anzahl der Protonen im Atomkern und das Element wandelt sich durch den Zerfall in ein anderes Element um. Sehr häufig wird diese Umwandlung (Zerfall) von der Aussendung von Strahlung begleitet, der erwähnten Gamma-Strahlung.
Was ist nun so besonders an der Gamma-Strahlung, dass wir uns mit ihr so intensiv beschäftigen?
Da ist zum einen die Tatsache, dass es sich um eine elektromagnetische Strahlung handelt, ähnlich wie beispielsweise das sichtbare Licht. Gamma-Strahlung hat aber eine wesentlich höhere Energie. Damit kann sie Materialien durchdringen und hierbei chemische oder biologische Bindungen oder Strukturen beschädigen,, weshalb beim Umgang mit Gamma-Strahlung ein wichtiger Aspekt der Strahlenschutz ist (d. h. wie kann man sich vor möglichen gesundheitsschädlichen Auswirkungen von Gamma-Strahlung schützen), sie aber auch für viele verschiedene Anwendungen eingesetzt werden kann (z. B. Radiographie, Tomographie etc.). Zum anderen hat die beim Zerfall eines Isotops ausgesandte Gamma-Strahlung nur ganze bestimmte (diskrete) Energien, die für jedes Isotop charakteristisch sind.
Haben Sie den Inhalt des letzten Satzes genau gelesen und sind Ihnen die darin steckenden Folgerungen klargeworden?
Falls nicht, hier die Zusammenfassung:
Wenn wir eine Möglichkeit finden die Energie der Gamma-Strahlung zu bestimmen, die beim radioaktiven Zerfall eines Isotops ausgesandt wird, dann können wir sagen, welches Isotop zerfallen ist. Wir hätten dann prinzipiell die Möglichkeit radioaktive Isotope zu identifizieren!
Diese Folgerung führt uns unmittelbar zum zweiten Begriff, die Spektrometrie:


